Sáng 9-12, đơn vị nghiên cứu vaccine ngừa Covid-19 đầu tiên của Việt Nam báo cáo kết quả nghiên cứu tiền lâm sàng với Hội đồng Đạo đức của Bộ Y tế để xem xét được khởi động giai đoạn 1 thử nghiệm vaccine trên người.
Phóng viên Báo Nhân Dân điện tử có cuộc trao đổi với TS Nguyễn Ngô Quang, Phó Cục trưởng Cục Khoa học công nghệ và Đào tạo, Bộ Y tế về lộ trình thử nghiệm vaccine ngừa Covid-19 trên người của Việt Nam.
Điều kiện tham gia thử nghiệm lâm sàng
PV: Việt Nam chính thức thử nghiệm vaccine ngừa Covid-19 giai đoạn 1 bắt đầu từ ngày 10-12. Xin ông cho biết về những kết quả nghiên cứu tiền lâm sàng của vaccine ngừa Covid-19 đầu tiên ở Việt Nam được đưa vào thử nghiệm lâm sàng?
TS Nguyễn Ngô Quang: Những nghiên cứu tiền lâm sàng, trong đó có phát triển chủng virus, quy trình sản xuất, kiểm tra chất lượng và thử nghiệm tiền lâm sàng là những quy trình chặt chẽ và yêu cầu phải bảo đảm các khía cạnh về mặt khoa học. Trên cơ sở đó, Hội đồng Đạo đức của Bộ Y tế mới thẩm định và quyết định có thông qua hay không.
Để có thể triển khai một sản phẩm nói chung, vaccine nói riêng cho phép triển khai trên người, bắt buộc chúng ta phải có nghiên cứu tiền lâm sàng.
Đối với vaccine có năm quy trình: Một là xây dựng ngân hàng tế bào; Hai là phát triển chủng virus; Ba là phát triển công nghệ và quy trình sản xuất; Bốn là kiểm tra chất lượng; Năm là báo cáo hồ sơ thử nghiệm hay là các kết quả đánh giá tiền lâm sàng.
Trong quy trình này, bốn nội dung ban đầu khá là chuyên sâu. Riêng với nội dung thứ 5 - kết quả đánh giá tiền lâm sàng, cơ quan quản lý yêu cầu có ba nội dung chính cần có hồ sơ minh chứng: Một là đánh giá tính sinh miễn dịch; Hai là kết quả đánh giá về an toàn và độc tính; Ba là đánh giá về test thử thách và đánh giá hiệu lực.
Đến nay, vaccine do Công ty TNHH Công nghệ sinh học Dược NANOGEN sản xuất đã hoàn thành xong các kết quả nghiên cứu tiền lâm sàng về tính sinh miễn dịch và đã được Viện Vệ sinh Dịch tễ Trung ương khẳng định, có báo cáo kết quả bằng văn bản gửi Hội đồng Đạo Đức của Bộ Y tế.
PV: Người tham gia thử nghiệm lâm sàng sẽ được tuyển chọn như thế nào?
TS Nguyễn Ngô Quang: Giai đoạn 1, dự án sẽ lựa chọn các tình nguyện viên. Đây là người tham gia tình nguyện theo nguyện vọng của cá nhân, không có áp lực nào. Nhóm nghiên cứu sẽ cung cấp một bảng cung cấp thông tin về nghiên cứu, trong đó có các nội dung: mục tiêu nghiên cứu, số lượng nghiên cứu, yêu cầu đánh giá nghiên cứu, các yêu cầu tham gia với người tình nguyện...
Sau khi người tình nguyện đọc kỹ, trao đổi với các thành viên nhóm nghiên cứu, người tình nguyện sẽ phải ký giấy chính thức cam kết đồng thuận tham gia và hoàn toàn tình nguyện tuân thủ theo các yêu cầu.
Bên cạnh việc tham gia thử nghiệm tình nguyện thì người đăng ký tham gia phải đáp ứng những tiêu chí về mặt y tế là người khỏe mạnh; Các chỉ số liên quan đến sinh học thông qua các kết quả đánh giá về huyết học và sinh hóa hoàn toàn bình thường; Không có các bệnh mãn tính và được cơ quan y tế xác nhận hoàn toàn là người khỏe mạnh. Ngoài ra, một số các tiêu chí liên quan đến tính chất đặc thù thì Hội đồng Đạo đức sẽ thông qua.

Bảo đảm an toàn cho các đối tượng tham gia nghiên cứu
PV: Về mặt chuyên môn, kỹ thuật, quy trình thử nghiệm vaccine sẽ không rút ngắn, nhưng để đối phó với đại dịch Covid-19, Bộ Y tế cũng đã cho biết sẽ hỗ trợ đơn vị nghiên cứu rút ngắn về mặt thủ tục. Xin ông cho biết chúng ta sẽ rút ngắn các bước như thế nào?
TS Nguyễn Ngô Quang: Về mặt nguyên tắc, thử nghiệm lâm sàng vaccine là một nghiên cứu đòi hỏi về mặt thời gian, công sức, trung bình mất khoảng 7 - 12 năm. Tuy nhiên trong trường hợp khẩn cấp, hay trường hợp đại dịch, phục vụ cho an ninh y tế thì các quy trình có thể được rút gọn.
Tôi xin nhấn mạnh là chúng ta chỉ rút gọn về mặt quy trình thủ tục chứ không rút gọn, không giảm bớt các quy trình về mặt chuyên môn, kỹ thuật. Yêu cầu đặt ra là các nhà sản xuất vẫn phải trả lời được ba câu hỏi: vaccine thử nghiệm có bảo đảm tính an toàn, tính sinh miễn dịch và hiệu lực bảo vệ trong bao lâu.
Cơ quan quản lý và Hội đồng Đạo đức yêu cầu các nhà sản xuất phải bảo đảm đúng các tiêu chí trên, bảo đảm an toàn cho các đối tượng tham gia nghiên cứu trước khi đánh giá tính sinh miễn dịch và hiệu lực bảo vệ ra sao.
Căn cứ theo tình hình đại dịch hiện nay, căn cứ các nghiên cứu phát triển vaccine Covid-19 trên thế giới, căn cứ các năng lực đặc biệt của Việt Nam với hệ thống nghiên cứu phát triển vaccine là một trong số ít những quốc gia được WHO công nhận trong hệ thống quản lý phát triển vaccine quốc gia NRA, vaccine do NANOGEN đưa vào thử nghiệm (vaccine Nano Covax), dự kiến thử nghiệm lâm sàng trong khoảng 12- 14 tháng.
Theo chỉ đạo chung của lãnh đạo Bộ Y tế, chúng tôi phối hợp với nhà sản xuất NANOGEN và Học viện Quân y, dự kiến xây dựng đề cương nghiên cứu thử nghiệm lâm sàng vaccine Nano Covax với giai đoạn 1 từ tháng 1-2021 đến tháng 4-2021.
Ngày hôm nay, Hội đồng Đạo đức của Bộ Y tế sẽ họp và dự kiến khởi động cho dự án này vào ngày 10-12 tại Học viện Quân y.
PV: Xin ông có thể cho biết về quy trình tiêm thử nghiệm của Việt Nam trong thời gian tới đây?
Thử nghiệm vaccine lâm sàng có ba giai đoạn chính: Giai đoạn 1 thử nghiệm trên người tình nguyện khỏe mạnh, giai đoạn 2 thử nghiệm trên các đối tượng đích trên một số lượng hạn chế, giai đoạn 3 thử nghiệm cỡ mẫu tối thiểu khoảng 10 nghìn đến vài chục nghìn, đòi hỏi thời gian khá dài.
Thử nghiệm đánh giá ba mục tiêu chính là tính an toàn của vaccine, tính sinh miễn dịch của vaccine và hiệu lực bảo vệ của vaccine,
TS Nguyễn Ngô Quang: Sau khi rà soát lại hồ sơ nghiên cứu tiền lâm sàng và các nghiên cứu tương tự trên thế giới, dự kiến, chúng ta sẽ thử nghiệm hai khoảng liều chính là 50 microgam và 75 microgam.
Nếu được Hội đồng thông qua, dự kiến giai đoạn 1, chúng ta sẽ có khoảng 40 đối tượng tham gia. Đây là giai đoạn rất nhạy cảm và rất quan trọng, khi chuyển nghiên cứu từ động vật sang người.
Dự kiến từ tháng 1 - 4-2021, khi có kết quả ban đầu giai đoạn 1, đặc biệt đánh giá về tính an toàn của hai khoảng liều thì Hội đồng Đạo đức sẽ chuyển sang giai đoạn 2.
Dự kiến giai đoạn 2 sẽ tiến hành từ tháng 3 - 4-2021 và giai đoạn 2, số lượng cỡ mẫu tối thiểu là 400. Giai đoạn 2 bắt buộc phải thiết kế nghiên cứu có nhóm chứng, nghĩa là chúng ta sẽ sử dụng các đối tượng có nguy cơ, liên quan đến vùng dịch tễ và đối tượng thứ 2 là nhóm sử dụng thuốc đối chứng.
Trên cơ sở kết quả giai đoạn 1 thì cơ quan quản lý và Hội đồng Đạo đức mới cho phép triển khai kết quả giai đoạn 2, trên cơ sở kết quả giai đoạn 2 thì cơ quan quản lý và Hội đồng Đạo đức sẽ cho phép chuyển sang giai đoạn 3. Giai đoạn 3 dự kiến thử nghiệm với số lượng tối thiểu là 10 nghìn người vào khoảng tháng 8-2021.
Đặc biệt giai đoạn 3 rất cần việc triển khai, đánh giá vaccine trên đối tượng có nguy cơ cao hoặc dự tính đối với SARS-CoV-2 để đánh giá tính sinh miễn dịch.
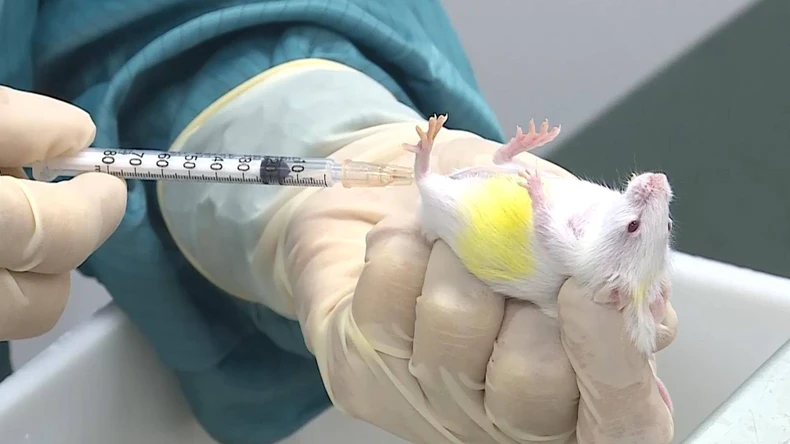
Việt Nam sẽ phối hợp với ba nước để triển khai nghiên cứu đa trung tâm giai đoạn 3
PV: Để đáp ứng được việc nghiên cứu ở giai đoạn 3, Việt Nam có kế hoạch như thế nào, thưa ông?
TS Nguyễn Ngô Quang: Hiện nay, Việt Nam phòng dịch rất tốt nên chúng tôi có những lo lắng liên quan đến đối tượng nghiên cứu thuộc đối tượng nguy cơ cao hoặc dương tính cho giai đoạn 3.
Tại cuộc họp Thường trực Chính phủ báo cáo Thủ tướng Chính phủ về công tác phòng, chống dịch Covid-19, Bộ trưởng Y tế cũng đã công bố chính thức là Việt Nam sẽ chính thức phối hợp với ba quốc gia Indonesia, Ấn Độ, Bangladesh để triển khai nghiên cứu đa trung tâm, để chúng ta làm sao có được số lượng bảo đảm cỡ mẫu tối thiểu là 10 nghìn. Theo báo cáo về mặt dịch tễ, đây là ba nước ở châu Á có tỷ lệ dịch tễ cao nhất.
Hiện nay, Bộ Y tế đã giao cho nhà sản xuất NANOGEN liên hệ với ba quốc gia này để có thể có những kết nối ban đầu. Bộ Y tế sẽ có văn bản chính thức gửi cho các cơ quan quản lý y tế của các quốc gia này để phối hợp với NANOGEN.
Mục tiêu phối hợp với các quốc gia để chúng ta tăng thêm cỡ mẫu và đặc biệt là số lượng đối tượng có dịch tễ cao, ở trong vùng dịch tễ để mình so sánh với nhóm nghiên cứu hoàn toàn không sử dụng vaccine, để đánh giá được hiệu lực của vaccine.
Như vậy, dự kiến thời gian nghiên cứu sẽ kéo dài từ tháng 1-2021 và chúng tôi hy vọng đến tháng 12-2021 thì chúng ta có các dữ liệu ban đầu về an toàn tính sinh miễn dịch.
Tuy nhiên, để đánh giá khả năng bảo vệ hay hiệu lực bảo vệ của vaccine thì chúng ta còn phải thêm thời gian theo dõi tiếp theo vì trong 12 tháng, thậm chí 16 tháng chúng ta vẫn chưa đủ thời gian để đánh giá được hiệu lực bảo vệ.
PV: Xin ông cho biết thêm về nguồn vốn hỗ trợ các đơn vị nghiên cứu?
TS Nguyễn Ngô Quang: Về kinh phí nghiên cứu, các đơn vị tham gia nghiên cứu vaccine ngừa Covid-19 sẽ được Chính phủ Việt Nam đầu tư. Sau NANOGEN, chúng ta cũng sẽ có hai vaccine tiềm năng để có thể tiếp tục triển khai thử nghiệm lâm sàng. Như vậy, Việt Nam chúng ta có ít nhất ba vaccine ở trong nước được nghiên cứu phát triển và dự kiến sẽ triển khai thử nghiệm lâm sàng trong năm 2021.
Chúng tôi hy vọng rằng những nghiên cứu thử nghiệm lâm sàng sớm có những kết quả ban đầu. Dự kiến vào tháng 1-2022, Việt Nam có thể có được vaccine do chính người Việt Nam nghiên cứu sản xuất để phục vụ cho cộng đồng.
Xin cảm ơn TS Nguyễn Ngô Quang!
- Tháng 3-2021, vaccine ngừa Covid-19 thứ 2 của Việt Nam sẽ được thử nghiệm
- Lộ trình thử nghiệm vaccine ngừa Covid-19 tại Việt Nam
- Đầu năm 2021, vaccine ngừa Covid-19 có thể thử nghiệm trên người
- Bài toán phân phối và tiêm chủng vaccine ngừa Covid-19
- Bao giờ Việt Nam tiếp cận được vaccine ngừa Covid-19?